南通高效細胞周期檢測服務
細胞模型構建技術是研究復雜細胞現象的有力工具,能模擬真實細胞情境。三維細胞培養技術打破傳統二維培養的局限,利用生物材料支架或微流控芯片構建類似體內組織的三維結構,使細胞間及細胞與基質間相互作用更自然,用于瘤子微環境模擬、藥物篩選等。類部位培養技術更是一大突破,從人體組織或干細胞誘導生成具有部位特異性結構和功能的類部位,如腸道類部位、腦類部位,為研究部位發育、疾病發生機制提供前所未有的平臺,縮短實驗室與臨床應用距離,讓細胞研究成果更快惠及人類健康。細胞生物學技術服務提供單細胞測序服務,深入剖析細胞異質性,挖掘細胞奧秘。南通高效細胞周期檢測服務
以細胞培養為例,首先要獲取合適的細胞來源,如從組織中分離原代細胞或使用已建立的細胞系。對獲取的細胞進行復蘇(若為凍存細胞),將其接種到含有適宜培養液的培養器皿中,置于培養箱中培養。培養過程中,需定期觀察細胞的生長狀態,根據細胞密度進行傳代培養。當需要進行細胞轉染時,先將外源核酸與轉染試劑混合形成復合物,然后加入到培養的細胞中,孵育一定時間,使復合物進入細胞。對于熒光標記實驗,先將熒光探針與目標分子結合,再將其加入細胞培養液中,待標記完成后,在熒光顯微鏡下進行觀察和成像。每個實驗流程都需嚴格遵守無菌操作原則,確保實驗結果的準確性和可靠性。嘉興細胞侵襲檢測服務應用細胞生物學技術服務助力制藥企業,高效篩選藥物靶點,加速新藥研發進程。
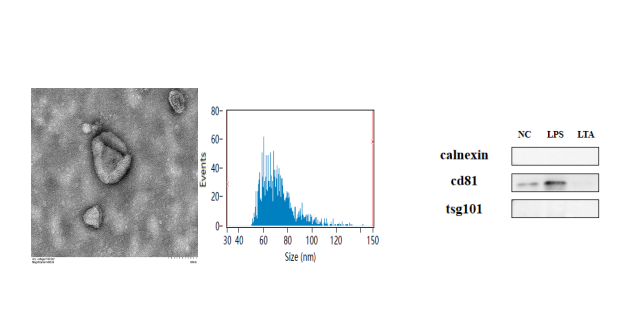
細胞遷移與侵襲能力的研究對瘤子轉移、組織修復等領域意義重大。劃痕實驗是簡單直觀的方法,在細胞單層上制造劃痕,觀察細胞向劃痕區域遷移的情況,通過顯微鏡拍照記錄不同時間點的細胞遷移距離,進行量化分析。Transwell 實驗則更為精確,上室加入細胞,下室加入含有趨化因子的培養液,細胞會向趨化因子濃度高的方向遷移。對于侵襲實驗,還需在 Transwell 小室的聚碳酸酯膜上鋪上一層基質膠,模擬體內細胞外基質,檢測細胞穿過基質膠和聚碳酸酯膜的能力。實時細胞分析技術(RTCA)利用微電極傳感器實時監測細胞遷移過程中電阻抗的變化,可動態、定量地分析細胞遷移和侵襲行為。
細胞分離與純化旨在從復雜的細胞群體中獲取單一類型的細胞,以滿足不同研究和應用的需求。常用的方法包括離心技術,根據細胞的大小、密度等物理特性,通過不同速度的離心將不同類型的細胞分離開來。例如,差速離心可將紅細胞與白細胞初步分離,因為紅細胞的密度較大,在較低的離心速度下就會沉淀下來。流式細胞術則是一種更為精確的細胞分離和分析方法,它利用細胞表面或內部的特異性標志物,通過熒光標記的抗體與細胞結合,然后在流式細胞儀中根據細胞的熒光信號強度和散射光特性對細胞進行分選和計數。這一技術在免疫學研究中廣泛應用,能夠從血液或淋巴組織中分離出特定的免疫細胞亞群,如 T 淋巴細胞、B 淋巴細胞等,進一步研究它們的功能和特性,對于疾病的診斷和醫療具有重要意義。細胞生物學技術服務通過蛋白質印跡技術,檢測細胞內蛋白質表達與修飾。

干細胞技術是細胞生物學領域的前沿研究方向之一。干細胞具有自我更新和分化為多種細胞類型的能力。胚胎干細胞來源于早期胚胎,具有全能性,能夠分化為人體的各種細胞、組織和補位,在再生醫學領域具有巨大的潛在應用價值,例如可用于修復受損的心臟組織、神經組織等,但由于其來源涉及倫理問題,應用受到一定限制。成體干細胞存在于成體組織中,如骨髓間充質干細胞、神經干細胞等,具有多向分化潛能,可用于醫療一些退行性疾病和組織損傷。誘導多能干細胞(iPS 細胞)技術通過將特定的轉錄因子導入成體細胞,使其重編程為類似胚胎干細胞的狀態,為疾病模型的建立和藥物篩選提供了新的平臺。例如,利用患者的體細胞誘導生成 iPS 細胞,然后分化為疾病相關的細胞類型,用于研究疾病的發病機制和篩選醫療藥物,具有廣闊的應用前景,但目前 iPS 細胞技術還面臨著一些安全性和效率問題需要解決。細胞生物學技術服務提供細胞活力檢測服務,評估細胞生理狀態與功能。蚌埠高效泌體研究整體服務
細胞生物學技術服務通過單細胞功能分析技術,深入研究單個細胞的生物學特性。南通高效細胞周期檢測服務
細胞自噬是細胞維持內環境穩態的重要 “自我清理” 機制,其研究技術不斷創新。透射電子顯微鏡作為 “金標準”,憑借超高分辨率捕捉到自噬體、自噬溶酶體的雙層膜結構,直觀證實自噬的發生。基于熒光蛋白標記的自噬標記物,如 LC3,通過熒光顯微鏡實時監測自噬流的動態過程,判斷細胞自噬活性。在神經退行性疾病領域,研究發現自噬功能障礙導致異常蛋白聚集,利用自噬誘導劑激發自噬,觀察細胞內病理蛋白清理情況,為疾病醫療尋找新靶點,有望延緩病情進展,開啟細胞內環境凈化新途徑。南通高效細胞周期檢測服務
- 湖州多種位點組織芯片用途 2025-05-09
- 蕪湖組織芯片免疫熒光哪家靠譜 2025-05-09
- 廈門組織芯片免疫組化特點 2025-05-09
- 徐州組織芯片免疫熒光定制 2025-05-08
- 多種位點組織芯片技術 2025-05-08
- 蘇州多種位點組織芯片定制 2025-05-08
- 組織芯片免疫熒光服務公司 2025-05-08
- 廈門化學遺傳技術特點 2025-05-08
- 合肥組織芯片免疫組化服務公司 2025-05-08
- 無錫多種位點組織芯片技術服務 2025-05-08
- 肇慶附近按摩椅 2025-05-08
- 龍華區標準體外診斷試劑專賣店 2025-05-08
- 咸陽活性益生菌使用方法 2025-05-08
- 自行使用咽鼓管吹張器**** 2025-05-08
- 北京硬體艙制造商 2025-05-08
- 重慶華龕細胞灌裝系統 2025-05-08
- 無菌檢查培養基的圖片 2025-05-08
- 北京5ml血清移液管定做 2025-05-08
- 龍崗區便宜的生物試劑服務熱線 2025-05-08
- 湖州恒壓集中供水系統輸送設備 2025-05-08