-
個性化需求,專屬服務(wù):海綿定制如何滿足多樣化市場-海綿定制
-
如何選擇合適的過濾綿:提升過濾效率與延長使用壽命-過濾綿
-
揭秘物流網(wǎng)格海綿:如何在運(yùn)輸中提供良好緩沖效果-網(wǎng)格海綿
-
寵物海綿爬梯:為寵物量身定制的沙發(fā)與床間通行神器-海綿爬梯
-
寵物友好家居設(shè)計:海綿爬梯讓沙發(fā)、樓梯、床觸手可及-海綿爬梯
-
如何挑選高效耐用的杯刷海綿:一份實(shí)用的購買指南-杯刷海綿
-
淘氣堡海綿材質(zhì)對比,哪種更適合你家孩子-淘氣堡海綿
-
海綿鞋擦:輕松去除鞋面污漬-海綿鞋擦
-
高效去除洗衣機(jī)內(nèi)毛發(fā):洗衣球海綿的神奇功效-洗衣球海綿
-
寵物海綿爬梯:安全、舒適且有趣-小型寵物海綿爬梯輔助器報價
楊浦區(qū)國際注冊eCTD服務(wù)價格
ANDA遞交: 按照ICH M4的CTD格式整理資料,并以eCTD格式遞交; 通過ESG通道遞交資料; 收到CDER的letter,說明資料已經(jīng)進(jìn)入FDA數(shù)據(jù)庫; 付GDUFA費(fèi),在資料遞交后的10日內(nèi)到賬; ANDA接收: 繳費(fèi)后,F(xiàn)DA初步審查資料的完整性,并會在60天給答復(fù)。 第一種情況是ANDA無缺陷,F(xiàn)DA給申請人發(fā)受理信(Acceptance Letter); 第二種情況是ANDA包含少于10個小缺陷,F(xiàn)DA將會通過電話、傳真、電子郵件等方式通知發(fā)布IR (信息請求函),讓申請人在7個日歷日內(nèi)改正,若未按時補(bǔ)充所有需要的資料,F(xiàn)DA將拒收該ANDA; 第三種情況是ANDA包含1個或者多個重大缺陷,或10個以上的小缺陷,F(xiàn)DA將拒收該ANDA; 注:如果這邊被拒收,只退75%的費(fèi)用。澳大利亞IND注冊申報相關(guān)技術(shù)支持。楊浦區(qū)國際注冊eCTD服務(wù)價格
電子簽章與傳輸安全 文件需經(jīng)AES-256加密后刻錄至不可擦寫光盤,并附MD5校驗(yàn)碼。光盤損壞或病毒污染將觸發(fā)重遞交流程,原載體按銷毀程序處理。 ?審評與核查協(xié)同 自2018年起,F(xiàn)DA要求提交兩套光盤分別用于審評和現(xiàn)場核查,2022年調(diào)整為“1套審評+1套核查+1套專項(xiàng)資料”模式,提升流程效率。 ?國際化兼容性增強(qiáng) 美國eCTD系統(tǒng)支持與歐盟、日本等地區(qū)的XML互操作性,但區(qū)域差異(如模塊1的標(biāo)簽要求)仍需人工適配。 ?未來通道創(chuàng) FDA計劃引入API接口支持企業(yè)系統(tǒng)直連,并探索基于云存儲的實(shí)時提交與審評,減少物理媒介依賴。浙江國產(chǎn)eCTD銷售電話美國eCTD注冊咨詢相關(guān)技術(shù)支持。
文件生命周期管理:eCTD支持文件替換(Replace)、刪除(Delete)等操作,而非增文件。例如,更臨床研究方案時需用Replace操作覆蓋舊版本。基線提交(Baseline Submission)可用于補(bǔ)充歷史紙質(zhì)資料,但需在封面函中聲明無內(nèi)容變更。 臨床數(shù)據(jù)與研究標(biāo)簽文件(STF):模塊4和5中的研究數(shù)據(jù)需通過STF(Study Tagging Files)引用,確保數(shù)據(jù)與文檔關(guān)聯(lián)。FDA要求數(shù)據(jù)集(如SAS XPORT格式)能置于模塊3-5,且單個文件超過4GB需拆分。2022年統(tǒng)計顯示,58%的ANDA因研究數(shù)據(jù)技術(shù)拒絕標(biāo)準(zhǔn)(TRC)錯誤被拒。 電子簽名與表格要求:FDA表格(如356h、1571)需使用數(shù)字簽名,PDF文件禁止加密或設(shè)置編輯限制。電子簽名需符合21 CFR Part 11規(guī)范,確保身份驗(yàn)證、不可否認(rèn)性和數(shù)據(jù)完整性。 外包服務(wù)與系統(tǒng)解決方案:賦悅科技累計提交超2000份eCTD申請,外包可降低40%人工錯誤率。
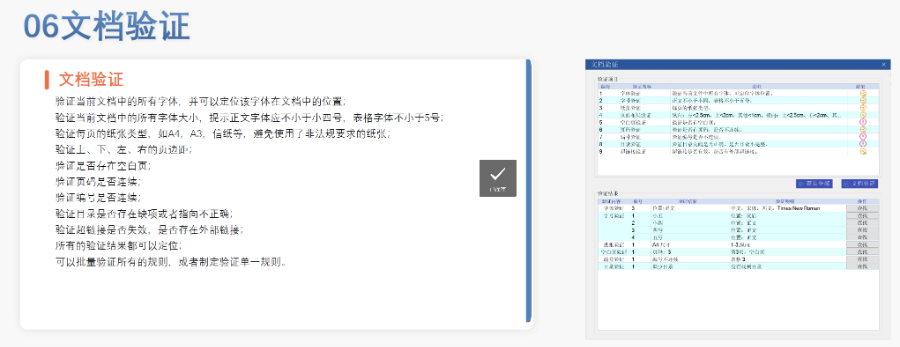
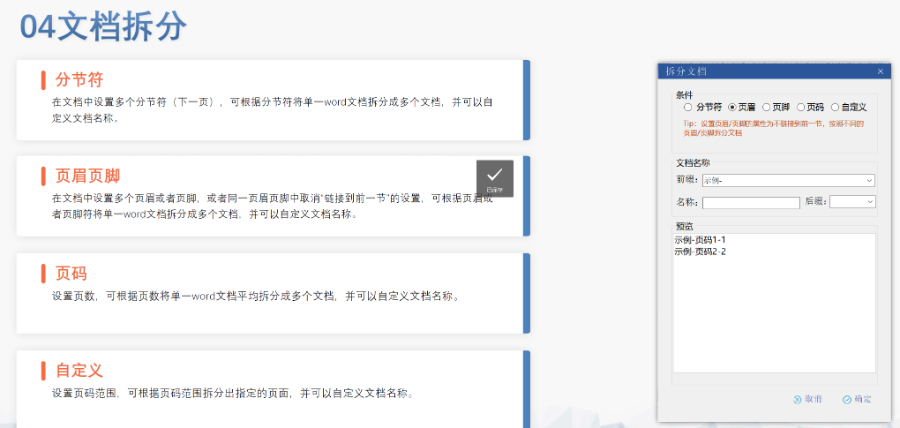
賦悅Word插件 自主研發(fā)Word插件 快速編輯:整合word常用功能按鈕,避免頻繁切換菜單;內(nèi)置標(biāo)題、段落、文字、目錄、超鏈接等的格式和樣式,可快速設(shè)置和更文檔的格式 快速鏈接:雙擊或者拖拽的方式,制作文本超鏈接或者題注超鏈接;可搜索全文關(guān)鍵字,自動制作超鏈接 文檔拆分:可根據(jù)不同的條件將word文件顆粒化,如分節(jié)符、頁眉、頁腳、頁碼范圍和自定義頁碼等 PDF轉(zhuǎn)換:WORD轉(zhuǎn)PDF,自動判斷是否生成書簽,自動鑲嵌所有字體,生成PDF快速網(wǎng)頁瀏覽的PDF,確保生成的PDF所有屬性符合法規(guī)要求 文檔驗(yàn)證:驗(yàn)證文檔的字體、字號、紙張、頁面布局、空白頁、頁碼、編號、目錄、超鏈接等,并且可以定位驗(yàn)證結(jié)果 可定制:可根據(jù)用戶需求定制格式和樣式模板eCTD驗(yàn)證標(biāo)準(zhǔn)相關(guān)技術(shù)支持。
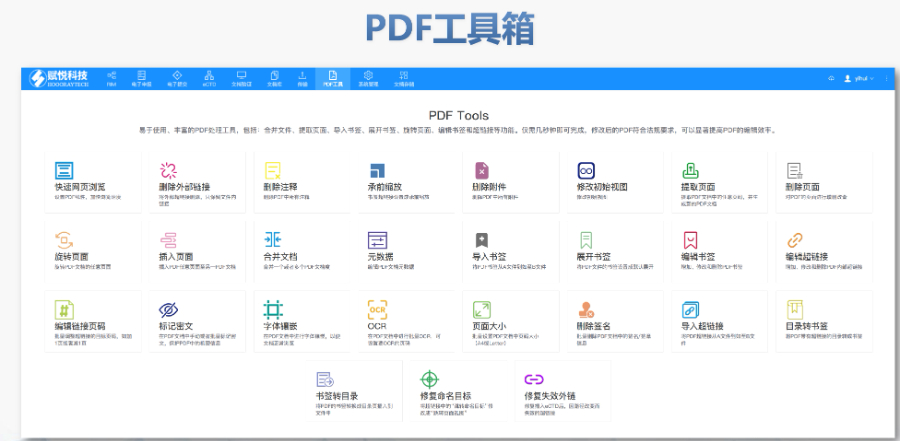
PDF工具箱 ?批量處理與格式修復(fù) 支持PDF合并、拆分、提取頁面、旋轉(zhuǎn)頁面等操作,可批量修復(fù)字體未嵌入、超鏈接錯誤等問題,確保文件符合藥品注冊法規(guī)要求。 ?智能書簽與超鏈接管理 提供書簽導(dǎo)入/導(dǎo)出、超鏈接自動生成(支持關(guān)鍵字搜索定位鏈接)、題注超鏈接拖拽式編輯等功能,簡化復(fù)雜文檔的導(dǎo)航設(shè)計。 ?文檔轉(zhuǎn)換與OCR識別 支持Word轉(zhuǎn)PDF(自動生成書簽、嵌入字體),以及PDF與Word、Excel等格式互轉(zhuǎn),集成OCR功能用于掃描件文字識別。 ?合規(guī)性驗(yàn)證 自動驗(yàn)證PDF的頁面布局、頁碼連續(xù)性、空白頁、目錄層級等屬性,并定位具體錯誤位置,減少人工檢查成本。 ?安全與協(xié)作功能 支持文檔加密、數(shù)字簽名、云端同步及多設(shè)備共享,滿足企業(yè)級文件安全管理需求。瑞士eCTD注冊咨詢相關(guān)技術(shù)支持。江蘇INDeCTD業(yè)務(wù)
澳大利亞eCTD申報軟件相關(guān)技術(shù)支持。楊浦區(qū)國際注冊eCTD服務(wù)價格
eCTD的技術(shù)架構(gòu)與模塊要求:美國eCTD基于XML技術(shù),嚴(yán)格遵循ICH M4框架,分為5個模塊:模塊1(地區(qū)行政信息)、模塊2(技術(shù)總結(jié))、模塊3-5(質(zhì)量、非臨床與臨床數(shù)據(jù))。其中,模塊1需包含F(xiàn)DA特定的文件,涵蓋申請編號、聯(lián)系人和DMF授權(quán)書等行政信息。模塊2-5需與ICH CTD全球統(tǒng)一標(biāo)準(zhǔn)一致,但FDA對文件顆粒度要求更細(xì),例如非臨床研究報告需拆分并標(biāo)記Study ID。PDF文件需符合FDA v4.1格式規(guī)范,包括字體嵌入、書簽層級和超鏈接功能。楊浦區(qū)國際注冊eCTD服務(wù)價格
- 太倉CDE eCTD注冊系統(tǒng) 2025-04-17
- 高新區(qū)CDE eCTD使用 2025-04-17
- 浦東新區(qū)藥品注冊eCTD服務(wù)價格 2025-04-17
- 浙江國內(nèi)注冊eCTD服務(wù)放心可靠 2025-04-16
- 工業(yè)園區(qū)賦悅科技eCTD文件如何制作 2025-04-16
- 工業(yè)園區(qū)生物制品eCTD發(fā)布系統(tǒng) 2025-04-16
- 杭州國產(chǎn)eCTD名稱 2025-04-16
- 安徽電子申報eCTD報價 2025-04-16
- 安徽電子申報eCTD歡迎選購 2025-04-16
- 安徽仿制藥eCTD名稱 2025-04-16
- 柳州數(shù)字檔案庫房哪家好 2025-04-17
- 懷柔區(qū)現(xiàn)代網(wǎng)絡(luò)測速操作 2025-04-17
- 威力科學(xué)減脂28天養(yǎng)成易瘦體質(zhì)規(guī)定 2025-04-17
- 吉林ANSYS 流體仿真 2025-04-17
- 天津電商平臺代運(yùn)營類型 2025-04-17
- 質(zhì)量SaaS智能營銷云平臺廠家供應(yīng) 2025-04-17
- 江陰電商平臺代運(yùn)營型號 2025-04-17
- 深圳旗艦工作站公司 2025-04-17
- 連云港省電智慧用電電話 2025-04-17
- 吉林短視頻營銷平臺 2025-04-17